prečo si vybrať nás
Certifikácie
Kaibang je nesmierne hrdý na to, že je držiteľom certifikátov ISO 9001:2015, ISO 14001:2015 a ISO 45001:2018, čo je dôkazom nášho neochvejného záväzku ku kvalite, efektívnosti, flexibilite a nákladovej konkurencieschopnosti.
Jednorazová služba
Sme profesionálny výrobca farmaceutických medziproduktov integrujúcich výskum a vývoj, výrobu a predaj.
Konkurenčná cena
Máme profesionálny nákupný tím a tím kalkulácie, ktorý sa snaží znížiť náklady a zisky a poskytnúť vám dobrú cenu.
Výrobné zariadenia
Venovali sme množstvo zdrojov na údržbu a udržiavanie našich zariadení v najlepšom stave pre našich zákazníkov.
Fluórfenol je organická zlúčenina s chemickým vzorcom C6H5FO. Je to aromatická zlúčenina s fluórovým substituentom na kruhu. Táto zlúčenina je dôležitou priemyselnou chemikáliou a používa sa hlavne pri výrobe iných chemikálií, ako sú liečivá, agrochemikálie a farbivá.
Aké sú aplikácie fluórfenolu
Farmaceutické prípravky
Fluorofenol je jedným z kľúčových medziproduktov pri výrobe niekoľkých liečiv, ako je fentikonazol, antifungálne činidlo, ktoré sa používa na liečbu kožných infekcií. Používa sa aj pri vývoji iných liekov, ako sú agonisty Toll-like Receptor 9 (TLR9).
Agrochemikálie
Mnoho agrochemikálií, ako sú herbicídy a insekticídy, používa 3-fluórfenol ako medziprodukt. Používa sa aj pri výrobe abamektínu používaného ako pesticíd.
Farbivá
Fluórfenol sa používa ako medziprodukt pri výrobe farbív, ako je etylfialová, ktorá nachádza uplatnenie v textilnom priemysle. Fluórfenol je životne dôležitá zlúčenina v chemickom priemysle so širokým využitím ako medziprodukt pri syntéze rôznych liečiv, agrochemikálií a farbív.
Druhy fluórfenolu

2,3,4,5,6-pentafluórfenol
2,3,4,5,6-Pentafluórfenol je polyfluórovaná zlúčenina z tekutých kryštálov s malým priestorovým odporom, ktorá je dôležitým medziproduktom pri príprave vysokovýkonných materiálov z tekutých kryštálov, zvlášť vhodných na prípravu polyfluórovaného monoméru materiály z tekutých kryštálov.
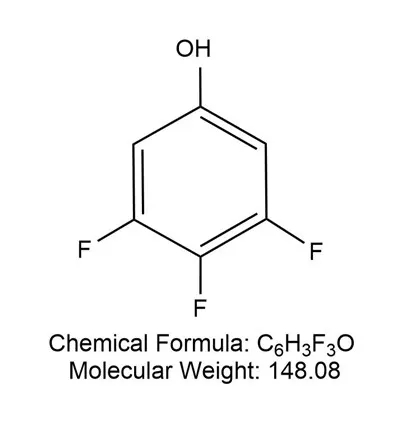
3,5-difluórfenol
3,5-Difluórfenol (DFP) je dôležitý chemický medziprodukt, ktorý našiel široké využitie vo farmaceutickom, agrochemickom a materiálovom priemysle. Táto biela kryštalická pevná látka má chemický vzorec C6H4F2O a molekulovú hmotnosť 146,1 g/mol.


3-Fluórfenol
3-Fluórfenol je organická zlúčenina s chemickým vzorcom C6H5FO. Je to aromatická zlúčenina s fluórovým substituentom na kruhu. Táto zlúčenina je dôležitou priemyselnou chemikáliou a používa sa hlavne pri výrobe iných chemikálií, ako sú liečivá, agrochemikálie a farbivá.
2,3,4,5,6-pentafluórfenol CAS NO.771-61-9
Pentafluórfenol, tiež známy ako 2,3,4,5,6-pentafluórfenol alebo PFP, je bezfarebná až svetložltá kryštalická pevná látka, ktorá patrí do skupiny fluórovaných derivátov benzénu. Táto zlúčenina má molekulový vzorec C6HF5O a molekulovú hmotnosť 186,06 g/mol.

Štrukturálne vlastnosti fluórfenolu
Fluórfenol sa môže použiť ako aromatická zlúčenina a ako derivát fenolu a jeho chemické vlastnosti sú podobné fenolu. Môže reagovať s kyselinami alebo zásadami za vzniku zodpovedajúcich solí. Môže podstúpiť oxidačnú reakciu pôsobením oxidačného činidla, aby sa vytvorila zodpovedajúca zlúčenina fenolftaleínu.
Chemické vlastnosti fluórfenolu
| Bod topenia | 16,1 stupňa (lit.) |
| Bod varu | 171-172 stupeň /741 mmHg (rozsvietený) |
| Hustota | 1,256 g/ml pri 25 stupňoch (lit.) |
| Index lomu | n20/D 1.511 (lit.) |
| Fp | 116 stupňov F |
| Skladovacia teplota | Inertná atmosféra, izbová teplota |
| Rozpustnosť | 37.7g/l |
| Formulár | Kvapalina |
| Pka | 8,73 (pri 25 stupňoch) |
| Špecifická gravitácia | 1.256 |
| Farba | Číry bezfarebný až svetložltohnedý |
| Rozpustnosť vo vode | 80.72g/L(25 ºC) |
| BRN | 1905112 |
| Stabilita: | Stabilný. Horľavý. Nekompatibilné so silnými oxidačnými činidlami. |
| InChIKey | HFHFGHLXUCOHLN-UHFFFAOYSA-N |
| Odkaz na databázu CAS | 367-12-4(Referencia databázy CAS) |
| NIST Chémia Referencie | Fenol, 2-fluór-(367-12-4) |
| Systém registra látok EPA | o-fluórfenol (367-12-4) |
Spôsob syntézy fluórfenolu
V suchom 10 ml reaktore sa zmieša 1 ekvivalent kyseliny p-fluórfenylborónovej (122 mg, 1 mmol), 2 ekvivalenty 30 % H202 (227 mg, 2 mmol) a 10 mg katalyzátora v 3 ml vody. Výsledná reakčná zmes sa miešala pri teplote miestnosti počas určitého časového obdobia a potom sa priebeh reakcie monitoroval pomocou TLC spotovej platne. Po dokončení reakcie sa reakčná zmes priamo extrahovala dietyléterom a vodou, organická vrstva sa oddelila a vysušila bezvodým síranom horečnatým a prefiltrovala, aby sa odstránila suchosť. činidlo, zvyšok po zahustení filtrátu možno oddeliť a vyčistiť stĺpcovou chromatografiou na silikagéli (5 % etylacetát rozpustený v petroléteri) a rozpúšťadlo sa odstráni na rotačnej odparke za zníženého tlaku, čím sa získa molekula cieľového produktu {{14 }}fluórfenol.
| Chemické vlastnosti | Číra bezfarebná až žltá kvapalina |
| Využitie | 2-Fluórfenol je kompetitívny inhibítor oxidácie 3,4-dihydroxyfenylalanínu (L-DOPA), katecholamínového prekurzora, ktorý sa používa ako terapeutické činidlo pre pacientov s Parkinsonovou chorobou. 2-Fluórfenol sa tiež používa ako jediný zdroj uhlíkovej energie pre baktérie. |
| Syntéza referencie | Tetrahedron, 52, s. 23, 1996 DOI: 10.1016/0040-4020(95)00867-8 |
| Journal of the American Chemical Society, 103, s. 1964, 1981 DOI: 10.1021/ja00398a015 | |
| Všeobecný popis | Kvapalná alebo kryštalická tuhá látka topiaca sa pri 14-16 stupňoch . Žieravý. Hustota 1,246 g / cm3. |
| Reakcie vzduchu a vody | Veľmi horľavý. |
| Profil reaktivity | 2-Fluórfenol reaguje ako slabá organická kyselina. Môže byť nekompatibilný so silne redukujúcimi látkami, ako sú hydridy, nitridy, alkalické kovy a sulfidy. Často sa vytvára horľavý plyn (H2) a reakčné teplo môže plyn zapáliť. Teplo vzniká aj acidobázickou reakciou so zásadami. Takéto zahrievanie môže iniciovať polymerizáciu organickej zlúčeniny. Sulfonuje sa veľmi ľahko (napríklad koncentrovanou kyselinou sírovou pri izbovej teplote). Reakcie vytvárajú teplo. Veľmi rýchlo sa nitruje, dokonca aj zriedenou kyselinou dusičnou. |
| Hazard so zdravím | AKÚTNE/CHRONICKÉ RIZIKÁ: Toxický a dráždivý. |
| Spôsoby čistenia | Nechajte o-fluórfenol prejsť aspoň dvakrát cez plynovú chromatografickú kolónu pre malé množstvá; inak sa frakčne destiluje pri zníženom tlaku. [Beilstein 6 I 97, 6 IV 770.] |
2-Trend a analýza trhu s fluórfenolom
2-Trh s fluórfenolmi sa v posledných rokoch výrazne rozrástol, pričom stúpajúci trend je spôsobený eskaláciou spotrebiteľského dopytu a technickým vývojom. 2-Trh s fluórfenolmi zaznamenal prudký nárast ponúk produktov, ktoré uspokojujú rôzne požiadavky a záujmy, keďže sektory prijímajú inovácie. Globálnej expanzii napomohli aj priaznivé ekonomické podmienky a strategické spojenectvá.
S plánovanou integráciou špičkových technológií a meniacou sa dynamikou trhu je výhľad do budúcnosti stále pozitívny. So zameraním na neustále zlepšovanie a orientáciu na klienta má 2-trh fluórfenolov dobrú pozíciu na to, aby pokračoval v raste a etabloval sa ako významná sila vo svetovej ekonomike.
V nadchádzajúcich rokoch bude svetový 2-trh fluórfenolov zaznamenať stabilný rast, poháňaný kombináciou neustáleho technologického pokroku, rastúceho povedomia o životnom prostredí a rastúcej potreby zefektívnenia prevádzky. Očakáva sa, že hráči z odvetvia sa budú koncentrovať na inováciu produktov, strategickú spoluprácu a geografickú expanziu, aby využili rozvíjajúce sa príležitosti na trhu.
Naša továreň
Shaoxing Kaibang New Material Technology Co., Ltd je spoločnosť integrujúca výskum a vývoj, výrobu, predaj, profesionálneho výrobcu farmaceutických medziproduktov, špecializujeme sa na vývoj a výrobu aktívnych farmaceutických medziproduktov (API) a farmaceutických medziproduktov a získala si povesť vedúceho dodávateľa inovatívnych, vysoko kvalitných chemikálií. Shaoxing Kaibang New Material Technology Co., Ltd má dobre zavedené výskumné a kilogramové laboratórium, ktoré slúži našim globálnym zákazníkom na úrovni niekoľkých gramov až kilogramov a tiež vykonáva vývoj procesov, má vlastnú výrobnú linku, pentafluórfenol, difluórfenol, tetrafluórbenzylalkohol atď. hlavné konkurenčné produkty, vysoko čistené, vysoko kvalitné, dobre oceňované ich zákazníkmi.




certifikát




FAQ
Otázka: Aká je rozpustnosť 4-fluórfenolu?
Otázka: Aká je hodnota pKa P-fluórfenolu?
Otázka: Prečo je para chlórfenol kyslejší ako para fluórfenol?
Otázka: Ktorý je kyslejší O fluórfenol alebo P fluórfenol?
Otázka: Na čo sa používa 2 fluórfenol?
Otázka: Aké je pKa 4-chlórfenolu?
Otázka: Je fluórfenol kyslý?
Otázka: Ovplyvňuje pKa lipofilitu?
Otázka: Ktorý z nasledujúcich je najmenej kyslý fluórfenol?
Otázka: Prečo je O fluórfenol najslabšia kyselina ako P a M fluórfenol?
Otázka: Prečo je O-chlórfenol kyslejší?
Otázka: Ktorý je najkyslejší CHF3?
Otázka: Aké je poradie kyslosti fluórfenolu?
Otázka: Na čo sa 2 4 dichlórfenol používa?
Otázka: Ktorý z nasledujúcich je najmenej kyslý fluórfenol chlórfenol?
Otázka: Na čo sa 2 6 dichlórfenol používa?
Otázka: Na čo sa 4-chlórfenol používa?
Otázka: Ktorý orbitál je najkyslejší?
Elektronegativita je schopnosť atómu priťahovať viazaný pár elektrónov. Je priamo úmerná percentuálnemu charakteru. Preto majú sp orbitály najvyššiu elektronegativitu. Sp je teda kyslejší, pretože kyslý charakter je definovaný aj z hľadiska prijímania elektrónov.
Otázka: Prečo je O-chlórfenol kyslejší ako fenol?
Otázka: Čo je kyslejšie O nitrofenol alebo O metoxyfenol Prečo?
Sme profesionálni výrobcovia a dodávatelia fluorofenolov v Číne, ktorí sa špecializujú na poskytovanie vysoko kvalitných prispôsobených služieb. Srdečne vás vítame, aby ste si kúpili fluórfenol za nízku cenu z našej továrne. Kontaktujte nás pre cenovú ponuku.
marža fluórfenolu, nákladovo efektívny fluorofenol, vývoz fluorofenolu